Amicus Therapeutics总部位于美国新泽西州,是一家专注于罕见代谢性疾病新药研发和商业化的生物技术公司。近日,该公司宣布美国食品和药物管理局(FDA)已授予Galafold(migalastat)123mg硬胶囊加速批准,该药是一种口服、精准医疗药物,用于体外检测证实存在特定α-半乳糖苷酶基因突变的法布里病(Fabry disease)成人患者的治疗。
Galafold是基于可使肾间质毛细血管细胞神经酰胺三己糖甘脂(globotriaosylceramide,GL-3)水平降低的数据通过加速审批通道批准,作为加速审批的一部分,Amicus公司将启动验证性IV期临床项目继续评估该药物。
具体而言,FDA已批准Galafold用于治疗多达348种GLA突变的法布里病。据估计,在美国大约有3000例法布里病患者,其中大约50%可接受Galafold治疗。此次批准,使Galafold成为美国市场治疗法布里病的首个口服药物,同时也是过去15年来获得美国FDA批准的首个法布里病创新疗法。
此次批准,主要基于关键性III期临床研究Study 011(又名FACETS)的疗效数据。该研究显示,与安慰剂相比,Galafold显著降低了肾间质毛细血管GL-3水平;安全性方面,Galafold最常见的副作用为头痛、鼻咽炎、尿路感染、恶心和发热。监管方面,Galafold曾获得美国FDA的孤儿药资格、快速通道资格及优先审评资格。值得一提的是,Galafold此前曾于2015年9月遭到了FDA拒绝。
Amicus公司董事长兼首席执行官John F. Crowley表示,Galafold获得美国FDA批准标志着一个历史性的时刻,该药将为携带特定GLA变体的法布里病患者带来15年来首个新的治疗方案,这一成果也体现了公司持续专注于罕见代谢性疾病新药研发以改善此类患者生存的坚定使命。
法布里病是一种X连锁的显性遗传性溶酶体贮积症,是由于GLA基因突变导致α-半乳糖苷酶A(α-Gal A)缺陷所致,该酶的主要生物学功能是降解溶酶体中的特定脂质,包括GL-3(又名Gb3)。α-Gal A酶活降低或缺失会导致GL-3在多种受累组织中积累,包括中枢神经系统、心脏、肾脏和皮肤。GL-3的渐进性积累被认为导致了法布里病的发生,同时带来包括疼痛、肾衰竭、心脏病及中风等在内的一系列问题。
法布里病是一种渐进性疾病,症状可在患者年幼时就出现,疾病严重程度可能因人而异,若不加以治疗,最终都会引起器官损伤,导致早期死亡。与普通人群相比,法布里病导致预期寿命大大缩短,女性患者平均寿命为15年,男性患者平均为20年。
Galafold的活性药物成分为migalastat,这是一种α-半乳糖苷酶A(α-Gal A)的口服药理学“分子伴侣”,能够选择性、可逆性地结合特定突变类型的α-Gal A酶,稳定这些功能失调的酶,促进其运输至溶酶体清除积累的疾病底物,从而发挥治疗作用。在全球范围内,据估计大约35%-50%的法布里病患者存在可治疗的GLA变体。之前,Galafold已获澳大利亚、加拿大、欧盟、以色列、日本、韩国、瑞士批准。
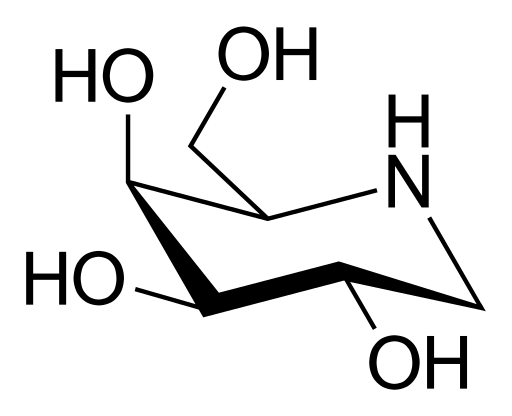
Migalastat分子结构(来自维基百科)
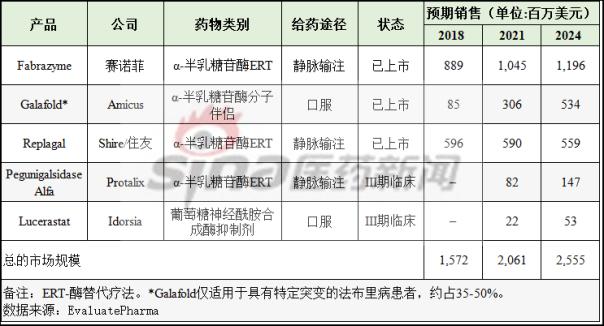
当前,法布里病的治疗方案是酶替代疗法(ERT),已上市产品包括赛诺菲的Fabrazyme和Shire/住友制药的Replagal,这2种药物需要每2周静脉输注一次,以减少肾脏脂质沉积。作为全球首个口服法布里病治疗药物,业界对Galafold的商业前景非常看好。EvaluatePharma预测,该药上市后,将在2024年达到5.6亿美元的销售额。
除了上述几个药物之外,处于后期临床研发阶段的新药还包括Protalix公司的Pegunigalsidase Alfa和Idorsia公司的lucerastat,前者是为植物细胞表达的重组、聚乙二醇化、交联的α-半乳糖苷酶-A候选药物,后者是一种口服葡萄糖神经酰胺合成酶抑制剂。
(新浪医药编译/newborn)